
图片来源:Unsplash
撰文|clefable
审校|不周
包括人类在内,动物体内有两个系统会像密集的线路一般遍布全身,分别是血液系统和神经系统。它们的重要性无需多言。但另一方面,由于血管具有四通八达的特点,各种威胁人体的病原体或者肿瘤,只要有机可乘,就会进入血液之中。因为这通常意味着发现一片新大陆,迎来丰富的资源和群体数量的暴涨。当然,它们也可能出师不利,遭遇免疫细胞,或者被特异性抗体围攻,最终尸骨无存。
相较于血液系统,如果病原体把神经系统当作一条路,那更像是“不走寻常路”。但考虑到这条路的终点似乎只有一个——大脑,只要到达,就能造成足够大的破坏。而存在这种偏好的病原体,也能引起人们特别的关注。其中最让我们恐惧的,当属阿米巴原虫和狂犬病毒。
沿神经元逆行
居住在淡水环境中的福氏耐格里阿米巴(Naegleria fowleri)能进入人的鼻子,突破人体最薄弱的神经屏障——嗅上皮(olfactory epithelium),并沿着嗅觉神经纤维爬行,最终感染人脑。春天来了,夏天也不会远,这里提醒大家千万不要在清洁程度未知的湖泊中游泳。
而狂犬病毒、1型单纯疱疹病毒等嗜神经病毒,更是演化出了高效利用神经元逆行,进而感染大脑的能力。值得一提的是,让我们感受尤为深刻,带来嗅觉失灵、脑雾等症状的冠状病毒,也具有类似的能力。

图片来源:Unsplash
2023年,美国埃默里大学的科学家在预印本平台bioRxiv公开了一项研究,发现人体内还存在一种沿着神经元逆行的新形式:他们发现,受饮食影响,动物体内的肠道细菌一有机会,也会通过类似的方式进入大脑。虽然它们并不会有急性的伤害,但由于这种机制长期存在于人或动物的肠道中,可能与如今很多神经系统疾病患病率升高有关。
不过好在,这种伤害仍然可以逆转。这项研究成果目前也已被《公共科学图书馆·生物学》(PLOS Biology)接受,并将于近日发表。
肠道真的漏了
此前的一些研究就发现,肠道细菌分泌的代谢物和毒素,会间接影响神经系统,导致神经退行性病变,推动阿尔茨海默病、帕金森病和孤独症等疾病的出现。埃默里大学的科学家很好奇,这些细菌是否有可能直接进入大脑,造成破坏。
他们曾观察一种肝病小鼠模型,受饮食影响,这些小鼠的肠道细菌组成会发生改变。于是,他们以此为基础,给这些小鼠喂食了高脂肪含量的饲料。这种饮食名为Paigen饮食,是专门为诱导小鼠产生动脉粥样硬化而调制的,里面的脂肪(主要来源是可可脂和椰子油等,能量超过了总卡路里的35%)、胆固醇含量较高,研究人员还添加了胆酸,以促进脂肪和胆固醇的吸收。不出意外,这些小鼠出现了非常明显的变化。
8天后,相比于正常饮食的小鼠,高脂饮食组小鼠的肠道细菌开始失调:乳杆菌减少,而另一些肠道共生菌,比如金黄色葡萄球菌、拟杆菌和阿克曼菌则明显增加。通过进一步评估,研究人员发现小鼠的肠道屏障(intestinal tract barrier)出现了渗漏。
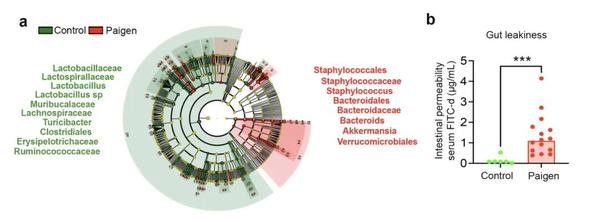
Paigen饮食和正常饮食小鼠的回肠和粪便主要细菌组成,以及肠道的渗漏情况 图片来源于bioRxiv论文
肠道屏障发挥的功能较为复杂,既需要帮助肠道细胞吸收各种营养物质,也需阻止无数想要进入人体的微生物。这都也决定了它的结构并不寻常。根据2024年一篇发表于《微生物学与生物技术杂志》(Journal Of Microbiology And Biotechnology)的综述性论文,肠道上皮细胞之间会有“紧密连接”(TJ)的结构等,可以阻碍肠腔内容物渗透。除此之外,其上部还有一层黏液层(MUCUS),其中含有碳酸氢盐、抗菌物质、糖蛋白和润滑剂等,形成了一个巨大的保护性环境。它们共同组成了肠道屏障。
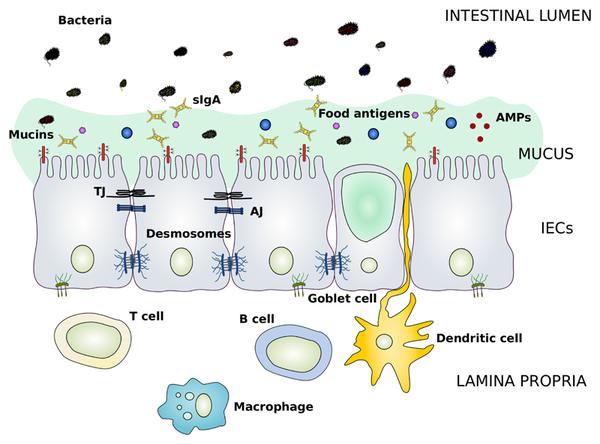
肠道屏障的组成 图片来源
论文中还揭示,随着高脂饮食改变肠道的细菌组成,细菌释放的一些内毒素物质会渗透进肠道,并进一步提高动物体内循环的内毒素。而整个过程会抑制构建“紧密连接”结构的多种蛋白质表达,肠道将会因此进一步渗漏。
树大根深的脑神经
如果细菌可以借此机会进入小鼠体内,它们可能去到哪里?埃默里大学的研究人员搜查了小鼠的血管、肺、心脏、肾脏、脾脏和大脑等。他们并未在血液和器官中找到细菌,但在大脑中找到了木糖葡萄球菌(staphylococcus xylosus)——这种细菌在小鼠的回肠和粪便也十分丰富。
通过比较血脑屏障的通透性,研究人员发现高脂饲料组的小鼠相比于正常饲料组,通透性并没有增加。因此,他们推测细菌进入大脑另有一条通道,而这让他们关注到了连接肠道和大脑的迷走神经。
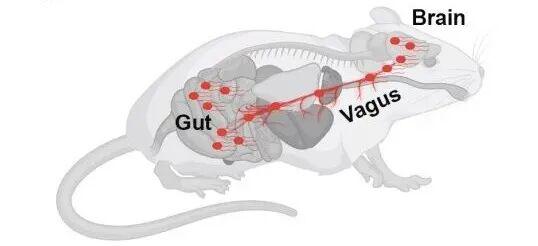
小鼠的迷走神经 图片来源于bioRxiv论文
迷走神经是动物体内最长的脑神经,有两根,它们就像大树一样,分别从身体的左右两侧出发,从脑干一直伸长到动物腹部的各个器官,能收集这些器官的感觉和运动信息,将它们传回大脑。迷走神经也是脑肠轴的核心,它能检测肠胃的饱腹感、肠道的免疫和炎症情况等等。
而就在迷走神经中,研究人员分离出了木糖葡萄球菌,但并未能从脊髓中分离出,这表明这些细菌可以特异性地转移到迷走神经。值得一提的是,左右两侧的迷走神经都可能会成为细菌进入大脑的通道。切除高脂饲料组小鼠单侧的迷走神经后(双侧都切,小鼠会死亡),研究人员观察到它们大脑中的细菌含量,相较于假手术组低约20倍,部分小鼠大脑中甚至没有检测到细菌。
随着研究人员进一步改变实验小鼠的种类,以及通过抗生素影响它们的肠道细菌,他们发现还有其他微生物也能采用类似方式,进入小鼠大脑。
比如C57BL/6小鼠是经过近百年的近亲繁殖培育而来,对高脂饮食也很敏感。它们经常作为研究糖尿病、肥胖症等疾病的模型。研究显示,高脂饮食喂养两周后,木糖葡萄球菌和粪肠球菌会在这类小鼠的肠道中聚集。与此同时,它们也会存在于小鼠的大脑。这也意味着,多种细菌甚至可以同时转移到大脑。
此外,研究人员发现,如果在小鼠的饮用水中添加抗生物混合物,其回肠和粪便中的灰芽孢杆菌(Paenibacillus cineris)的数量会增加,这种细菌也会转移到它们的迷走神经和大脑中。
改变饮食就能逆转
虽然在肠道中,这些细菌可能只是普通的共生菌,但由于出现在了不恰当的地方,比如大脑,它们就会变得有害。察觉到这些细菌之后,小胶质细胞会活化,触发大脑炎症。
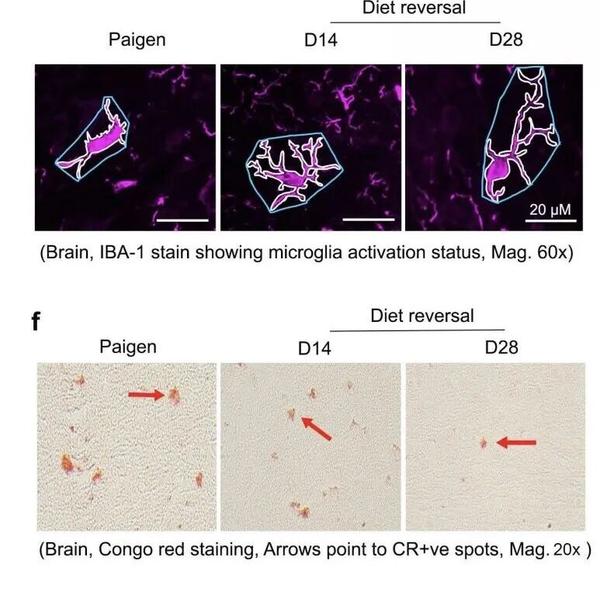
研究人员观察到,在大脑健康状态下,小胶质细胞会呈现为高度分支化的形态,而一旦大脑中出现炎症状况,它们就会活化,变成圆形、较小的变形虫样。在接受高脂饮食的肝病小鼠模型中,肠道细菌出现在大脑中,与小胶质细胞的活化,以及神经蛋白质聚集体的出现存在相关性。而一旦恢复常规饮食,就可充分逆转这种情况。
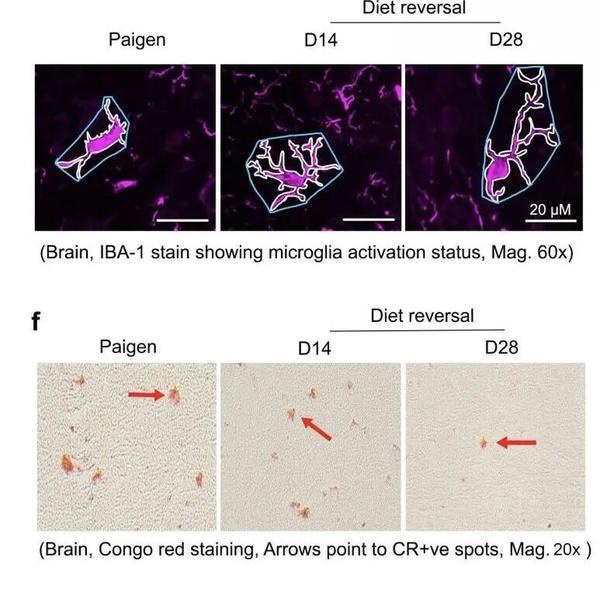
小鼠大脑中小胶质细胞的状态会随着饮食发生改变,在Paigen饮食的小鼠中呈现为明显的病理状态,但小鼠恢复正常饮食后,这些细胞又会恢复正常。图片来源于bioRxiv论文
当给小鼠喂食高脂饮食7天后恢复到普通饲料,研究人员发现在第14天,小鼠肠道的渗漏明显降低,而在小鼠回肠和大脑中几乎检测不到细菌,小胶质细胞的活化也被逆转,在第28天时,神经蛋白质聚集体的面积也明显降低。
不仅如此,这些发现似乎可以进一步推广到模拟人类阿尔茨海默病、帕金森病和孤独症而搭建的小鼠模型。患不同疾病的小鼠的肠道组成,会有较大差异,但它们都有一个明显的特点:肠道屏障被破坏。另一边,研究人员也在这些小鼠的大脑和迷走神经中,检测到了在它们回肠中较为丰富的细菌种类。
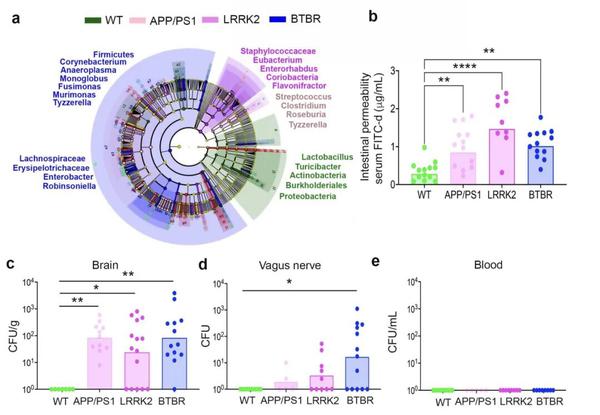
APP/PS1模型、LRRK2 模型和BTBR模型的小鼠分别对应阿尔茨海默病、帕金森病和孤独症。图片中显示了这些小鼠回肠和粪便中的主要细菌类群,肠道的渗透情况,迷走神经、大脑和血液中的细菌数量图片来源于bioRxiv论文
而这些疾病的结果,很可能是由早期肠道菌群和大脑的动态变化演变而来。这些发现也表明,连接肠和脑的迷走神经在这些大脑疾病中发挥了关键作用。而类似现象是否会发生在人类身上,以及这些细菌在神经系统疾病中可能扮演什么样的角色,还需要开展更多研究。
三种病理模型小鼠的小胶质神经细胞的形态。图片来源于bioRxiv论文
值得关注的可能不仅是肠道中的细菌。比如,科学家曾对比过阿尔茨海默病患者和健康对照者的死后脑组织,发现该疾病患者的大脑中存在多种真菌的遗传物质、蛋白质,甚至是真菌细胞体。
而根据2022年一项发表于《衰老神经科学前沿》(Frontiers in Aging Neuroscience)的研究,研究人员对无菌C57BL/6小鼠喂食一定剂量的白色念珠菌后,他们在小鼠的脑组织中,包括脑室、小脑、下丘脑、中脑和皮层,均发现了单个白色念珠菌细胞和细胞簇。
另一方面,他们并未在血管中发现这些真菌,这些发现也提示了白色念珠菌会主动侵袭脑组织。不过如果小鼠拥有肠道菌群,则可以抵御这种威胁。
正常来说,在包括人在内的动物体内,肠道中的微生物并不会造成太大威胁,甚至还有很大的益处。但一旦饮食长期失衡,比如长期采用高脂饮食,这些益处可能就会变为坏处。
参考链接:https://pmc.ncbi.nlm.nih.gov/articles/PMC11091682/
https://www.biorxiv.org/content/10.1101/2023.08.30.555630v1.full.pdf
https://www.frontiersin.org/journals/aging-neuroscience/articles/10.3389/fnagi.2022.828429/full#S3
https://feinstein.northwell.edu/news/insights/gut-brain-axis-vns
https://www.ncbi.nlm.nih.gov/books/NBK579780/?utm_source=chatgpt.com
