
撰文 | clefable
审校 | 冬鸢
1918年,当一战的形势逐渐明朗时,著名的物理学家爱因斯坦收到一位女性朋友的委托,希望他写信劝劝她当时在一个精锐骑兵团担任医生的儿子——让他重回学术界。这位母亲认为,失去儿子的才能会是这个世界的悲剧。13年后,这位医生不负所望,成为了当年唯一的诺贝尔生理学或医学奖的获得者。这个擅长马术的医生正是德国生物化学家奥托·海因里希·瓦尔堡(Otto Heinrich Warburg),他因为发现线粒体中“呼吸酶的性质和作用方式”于1931年获得了诺奖。

瓦尔堡的一生共获得了47次诺奖提名,而他在一生中都在研究两个基本的生物学问题:生命的能量是什么?以及癌细胞和正常细胞在代谢上的差异。如今来看,瓦尔堡极富远见,癌细胞的能量代谢至今都是科学界最受关注的领域之一。20世纪20年代,瓦尔堡曾发现癌细胞可以进行有氧糖酵解——在有氧的情况下,也能吸收大量葡萄糖产生乳酸。这个过程在它们的细胞质中进行,因此不需要线粒体,可以产能更快,可以让癌细胞实现快速增长。
当时,瓦尔堡认为,这是由于癌细胞线粒体异常或者缺陷导致的。不过后续的一些研究显示,癌细胞的线粒体可能并不会有明显缺陷,反而是缺少线粒体,会让它们的致癌性降低。一个观点则认为,肿瘤细胞拥有代谢可塑性,可以在糖酵解和氧化磷酸化(需要线粒体,产能更多)之间切换,以适应不同的生存挑战。
相比之下,人体内正常的细胞则非常依赖线粒体供能,而癌细胞似乎不仅知道这一点,还以此发现了打倒抗癌的T细胞的方式。3年前,美国哈佛医学院的副教授Shiladitya Sengupta的研究团队在《自然·生物技术》(Nature Biotechnology)上发表了一项研究。他们发现,癌细胞的体表会伸出多个“大手”,即长的纳米管道,以连接T细胞。这个举动充满敌意,它们会通过管道,偷走T细胞的线粒体。(点击阅读:首次发现:癌细胞竟能“伸出大手”,掏走免疫细胞的线粒体!)
科学家认为癌细胞对免疫细胞使出了一招“釜底抽薪”,而随着T细胞被“偷家”,它们也会失去战斗能力,从此一蹶不振。
或许是看到T细胞过于惨兮兮,今年9月,Sengupta的研究团队又在《细胞》(Cell)上发表了一篇论文。这次,他们为T细胞找到了一个能为其“超能充电”的后援。那么获得超能状态的T细胞对战癌细胞,胜算又有几何呢?
T细胞:完蛋,血条掉完了
当T细胞到达肿瘤周围时,肿瘤微环境中的多种分子,就会开始抑制T细胞的活性。而之后,T细胞更是会被偷走一些供能的线粒体,变得举步维艰,很快便走向了衰竭。这有点像是在反派大佬的压迫下,顶尖高手的装备、血量一顿狂掉,最后各种修炼的绝招完全没有机会发挥出来。
而这个过程似乎是不可逆的。科学家就曾发现如果将细胞中的线粒体全部去除,它们就无法产生新的线粒体。这个现象可以追溯到真核细胞中线粒体的起源。线粒体是真核细胞中一个关键的细胞器,内共生假说和现有的基因数据都证实,线粒体可能起源于阿尔法变形菌。线粒体也只能通过二元裂变形成,这正是细菌和古细菌使用的细胞分裂形式。
不过就算癌细胞会偷家,也不是全然没有希望。一些研究人员就观察到,一些细胞的线粒体可以转移到受损细胞中,促进受损细胞修复。这也让研究人员产生了一种新想法,给T细胞也输点线粒体,让它们恢复战斗力。
线粒体:一种战略资源
线粒体转移最主要的方式之一就是利用纳米管道。这种纳米管是细胞利用F-肌动蛋白形成的膜突起,它可以跨越很远的距离来桥接两个细胞。在这项新研究中,Sengupta和同事发现在人和小鼠体内,一种存在于人骨髓中的多能干细胞——骨髓间充质干细胞(BMSC)和CD8+ T细胞之间都会存在复杂的纳米管。其中BMSC会参与调节T细胞的功能和分化。

为了确定BMSC是否会向CD8+ T细胞输送线粒体,研究人员用人和小鼠的细胞分别进行了实验。他们先用红色荧光蛋白(DsRed)标记了BMSC中线粒体的亚基蛋白,再将BMSC和CD8+ T细胞共培养24小时后。结果发现,部分人和小鼠的CD8+ T细胞出现了红色荧光蛋白的信号。
研究人员还使用鬼笔环肽-绿色荧光(Phalloidin Green)对BMSC和CD8+ T细胞的F -肌动蛋白进行标记。当他们放大纳米管上的一些细节时,有了一个预期中的发现:绿色荧光的下面,有红色荧光标记的线粒体在移动。这也证实了研究人员的猜测,线粒体可以借由纳米管道,从BMSC运输到CD8+ T细胞。
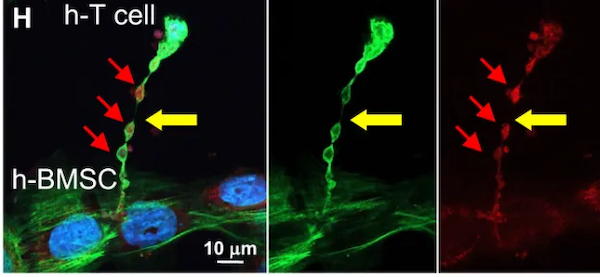
如果说,癌细胞和T细胞之间的纳米管是吸走T细胞能量的“巨大吸管”。那么,BMSC和CD8+ T细胞之间的则是一条紧急救援纳米管道,而在这些纳米管道的构建中,关键的TLN2基因发挥了重要作用。在CD8+ T细胞或BMSC中的TLN2缺失,都足以显著损害线粒体转移率。在BMSC中,这种影响尤为显著。
上擂台,“超能”T细胞!
线粒体的一个关键任务是通过有氧呼吸产生能量。研究人员发现,当CD8+ T细胞接受线粒体,会变身为拥有更高基础呼吸的“超能”T细胞,其备用呼吸能力(SRC)也会提高,可以帮助T细胞应对高能量代谢的情况。
而这些“超能”T细胞更能有效地进入肿瘤内部,而那些正常的T细胞仍然会被排除在肿瘤之外,只能在肿瘤外围发挥功能。在线粒体的加持下,这些“超能”T细胞的代谢率也不会受到肿瘤的明显影响。
小鼠实验显示,拥有“超能”T细胞的患癌小鼠的生存时间明显更长。这些“超能”T细胞在肿瘤微环境中更加活跃,发挥出了真正的杀伤能力,可以让肿瘤消退更快。研究人员表示,BMSC的线粒体对对抗肿瘤的CD8+ T细胞产生了深远的影响:让这些“超能”T细胞的存活率增加,拥有了强劲的、在肿瘤中扩张的能力。与此同时,它们对肿瘤引起的耗竭有了更强的抵抗力,且能变身为更具杀伤能力的“杀手”——高度特化的细胞毒性效应细胞。

更令人惊喜的是,这个效果并不是短暂的,而是可以长期存在。这些“超能”T细胞获得的线粒体可以通过重复分裂,传递给它们的子细胞。在转移过程发生1个月后,“超能”T细胞仍然拥有更多的线粒体。
这是一辆赛车
9月27日,一项发表于《转化医学杂志》(Journal of Translational Medicine)的研究也证实,线粒体转移可以逆转T细胞的命运轨迹,让它们对凋亡等死亡指令,拥有更高的抵抗能力。另外,如果将线粒体提供给能特异性抗癌的CAR-T细胞,这些细胞将会在人体存活更长的时间,发挥更强的抗癌能力。
巴西里约热内卢国家癌症研究所(INCA)的研究员、文章的共同作者之一Martín Hernán Bonamino表示,这就像是将一辆标准轿车改造成一辆赛车。那些接受了线粒体的CAR-T细胞不仅生存率提高,还具备了最佳的性能,能更有效地攻击癌细胞。
总的来说,一个最关键的决定因素是线粒体的结构和功能是否正常,而这和线粒体DNA的突变密切相关。大约60%的癌症病例发生在65岁及以上的患者中,而线粒体DNA发生累积损伤的可能性是核DNA的10倍。因此,癌症患者线粒体DNA中累积突变,可能会更多,而他们的线粒体是否正常,能否都发挥该有的作用,或许还是一个值得深入探究的问题。另外,研究人员较为担忧的一点是,在现有的转移过程中,线粒体转移率较低,大约为10%左右,这可能会影响这一方式后续在临床上的相关应用。
参考链接:
https://medicalxpress.com/news/2024-10-cellular-power-stem-cells-lifeline.html
https://translational-medicine.biomedcentral.com/articles/10.1186/s12967-024-05627-4
https://www.cell.com/cell/fulltext/S0092-8674(24)00956-5
https://www.nature.com/articles/s41565-021-01000-4
